技術情報
コア技術
1
画像:http://www.ueda.res.titech.ac.jp/html/page1_2.html
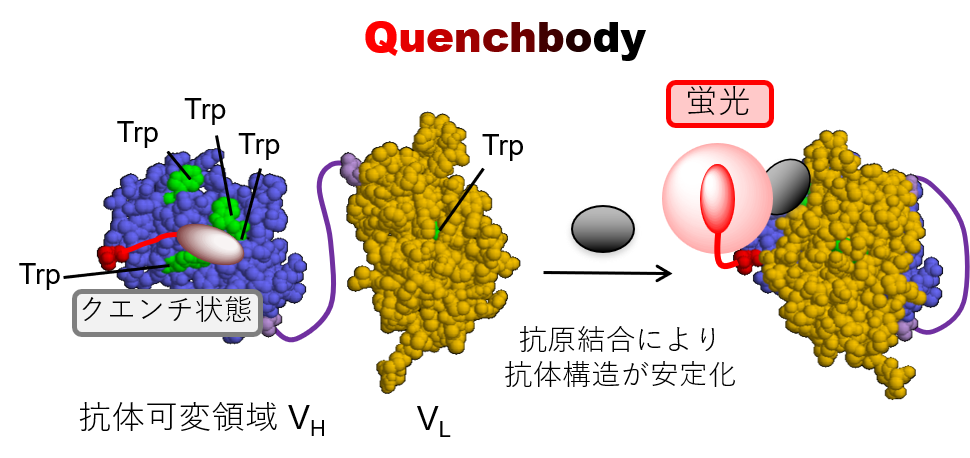
迅速簡便なバイオセンサー「Q-body」
免疫測定法は、夾雑物から測定したい物質のみを正確に、且つ、微量であっても検出できることから、臨床診断や食品検査の現場やラボなど様々な場面・分野で汎用されており、全世界で1,000億ドルの市場があります。しかし、「低分子抗原の検出は難しい場合が多い」、「測定工程が多く所要時間が非常に長い」、「その工程で洗浄工程とそのための洗浄装置が必要」などの問題もあります。
Q-bodyは、抗体の重鎖可変部位(VH)と軽鎖可変部位(VL)を結合させた単鎖可変領域(scFv)あるいは抗原結合断片(Fab)に、蛍光分子をリンカーで結合させ、VHとVLの間にその蛍光色素が内包化されている分子です。
この内包化により、VHの内部と表面に存在する複数のトリプトファンからの光誘起電子移動(PeT)が起こり、消光(クエンチ)状態を作り上げています。そして、抗原が結合すると、蛍光色素がVHとVLの間からはじき出され本来の蛍光を放つという仕組みです。
これにより、測定が洗浄工程(装置)不要な混ぜるだけの1工程になり、迅速簡便な免疫測定が可能になります。
2
画像:http://www.ueda.res.titech.ac.jp/html/page1_2.html
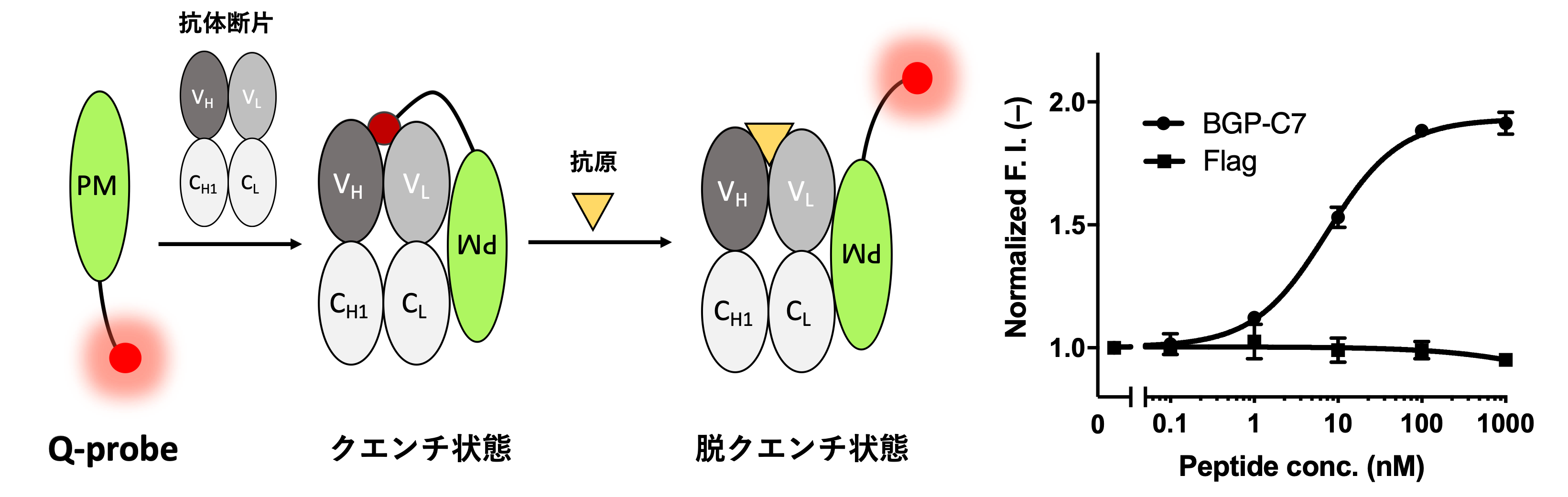
抗体選別方法「PM Q-probe」
抗体をQ-body化した際の応答性(クエンチ&脱クエンチの反応性)は、その抗体の持つ特性により様々です。これまで、望む応答性を持つ抗体の選別には、候補抗体すべてをQ-body化して評価するという工程のため、非常に多くの手間と時間を必要としていました。
そこで、近年、開発に成功したのが、抗体のL鎖に特異的に結合するプロテインMを用いて、効率的に抗体を選別する新技術PM Q-probeです。プロテインMと抗体を混ぜるだけで疑似Q-bodyを作成し、その応答性を評価するだけでその抗体がQ-bodyに適しているか選別することが可能になりました。
3
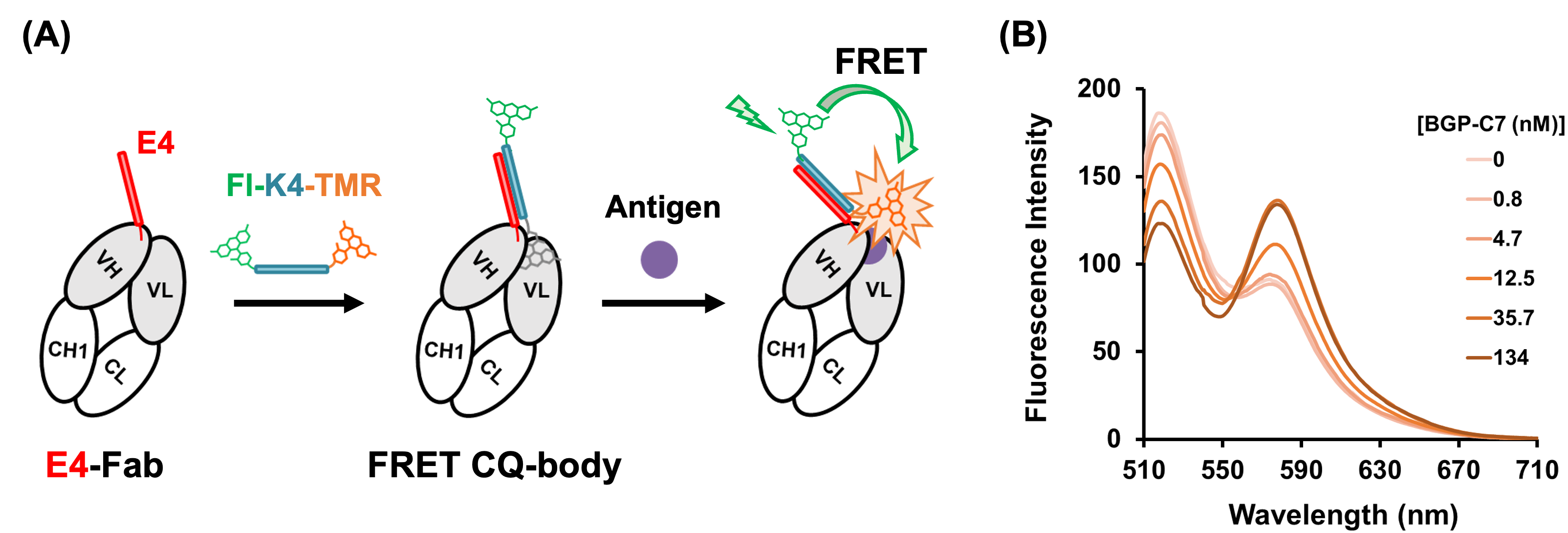
(A) 二色標識されたK4ペプチドを用いたFRET CQ-body構築の模式図。 (B) FRET CQ-bodyに抗原BGP-C7を添加したときの蛍光スペクトル。画像 + http://www.res.titech.ac.jp/news/reserch/202203u.html
測定精度及び保存性を向上させた改良型「Coiled Q-body」
旧型Q-bodyは安定性が高くないことが多く、キットにしても保存期間が数か月と、社会実装には非常に大きなハードルがありました。そこで、「構造が不安定であるならば、測定の直前にQ-bodyに合成すればいい」というアイデアのもと、開発したのがCoiled Q-bodyです。
互いにほぼ1対1で結合しあうヘリカルなE4ペプチドとK4ペプチドを用いて、”VHに結合させたE4”と”蛍光共鳴エネルギー移動(FRET)が起きるようペア色素を両端に結合させたK4”を、測定の直前に合体させます。このように抗体と色素を分けて保存することで、従来よりも安定性を高めました。これに加え、FRETにより片方の色素の蛍光輝度を基準とすることで、より正確な抗原の検出が実現可能となります。
技術開発者

上田 宏(うえだ ひろし)
東京工業大学 科学技術創成研究院
化学生命科学研究所 教授
1986年:東京大学工学部化学工学科卒業。1992年:同大学院工学系研究科博士課程修了、博士(工学)取得、工学部化学工学科助手。 1998年:英・ケンブリッジ大学MRC分子生物学研究センター客員研究員(ラムゼー記念奨学生)。 2013年:東京工業大学資源化学研究所教授、2022年12月23日ご逝去。
HikariQ/CTO

北口 哲也(きたぐち てつや)
東京工業大学 科学技術創成研究院
化学生命科学研究所 准教授
2001年:東京大学大学院医学系研究科博士課程修了、博士(医学)取得。2001年:米・国立衛生研究所研究員。 2005年:独・マックスプランク研究所研究員。2006年:京都大学医学研究科先端領域融合医学研究機構助手。 2011年:星・早稲田バイオサイエンスシンガポール研究所主任研究員。2018年:東京工業大学科学技術創成研究院化学生命科学研究所准教授。
HikariQ/R&D Managers

朱 博(しゅ はく)
東京工業大学 科学技術創成研究院
化学生命科学研究所 助教
2016年:名古屋大学大学院生命農学研究科生命技術科学専攻博士後期課程ならびにグリーン自然科学国際教育研究プログラム修了、博士号取得。同年:米・ミネソタ大学BioTechnology Institute博士研究員。 2018年:神戸大学大学院科学技術イノベーション研究科学術研究員。2020年:東京工業大学科学技術創成研究院化学生命科学研究所助教。

安田 貴信(やすだ たかのぶ)
東京工業大学 科学技術創成研究院
化学生命科学研究所 助教
2022年:東京工業大学生命理工学院ライフエンジニアリングコース博士後期課程ならびに文部科学省博士課程教育リーディングプログラム情報生命博士教育院課程修了、博士(工学)取得。同年:東京工業大学化学生命科学研究所助教。
その他応用例
A
臨床現場即時検査(発光酵素を活用し、抗原濃度を目視で確認)[4]
B
細胞の簡便な免疫染色[5][6]
C
RNA製剤への応用[5]
参考文献
[1] R. Abe, H. Ohashi, I. Iijima, M. Ihara, H. Takagi, T. Hohsaka, H. Ueda. J. Am. Chem. Soc. 133, 17386-17394 (2011)
[2] J. Dong, C. Miyake, T. Yasuda, H. Oyama, I. Morita, T. Tsukahara, M. Takahashi, J. Hee-Jin, T. Kitaguchi, N. Kobayashi and H. Ueda "PM Q-probe: a fluorescent binding protein that converts many antibodies to a fluorescent biosensor" Biosens. Bioelectron. 165, 112425 (2020).
[3] T. Yasuda, A. Inoue, T. Kitaguchi and H. Ueda "Rapid construction of fluorescence quenching-based immunosensor Q-bodies using α-helical coiled-coil peptides" Chem. Commun. 57, 8206-8209 (2021).
[4] R. Takahashi$, T. Yasuda$, Y. Ohmuro-Matsuyama and H. Ueda "BRET Q-Body : A Ratiometric Quench-based Bioluminescent Immunosensor Made of Luciferase–Dye–Antibody Fusion with Enhanced Response" Anal. Chem. 93, 21, 7571-7578 (2021).
[5] J. Dong$, Y. Oka$, H.-J. Jeong, Y. Ohmuro-Matsuyama and H. Ueda "Detection and destruction of HER2-positive cancer cells by Ultra Quenchbody-siRNA complex" Biotechnol. Bioeng. 117, 1259-1269 (2020).


